Не хочу искать, Вы всё равно останетесь при своем. У Вас останется, то православие которое вы создали в своём уме. Такова природа человека. Об этом даже написано в православной святоотеческой литературе.Голословные утверждения. Где доказательства? Я так могу сказать, что Кураев говорил, что Галицый носит роги на голове. И даже если бы он так сказал, то не факт, что это правда.
Вы используете устаревший браузер. Этот и другие сайты могут отображаться в нём некорректно.
Вам необходимо обновить браузер или попробовать использовать другой.
Вам необходимо обновить браузер или попробовать использовать другой.
эволюция
- Автор темы Семен23
- Дата начала
- Статус
- В этой теме нельзя размещать новые ответы.
Наблюдатель это душа. Про пассивного никто не говорит. Душа активна.Пассивный наблюдатель - это сатана, который и продвигает теорию эволюции. А Бог - это активный Творец!
- Православный христианин
И вот так все. Голословно и без доказательств.Не хочу искать, Вы всё равно останетесь при своем. У Вас останется, то православие которое вы создали в своём уме. Такова природа человека. Об этом даже написано в православной святоотеческой литературе.
- Православный христианин
Я не думаю, что душа человеческая наблюдала, как Бог создает мир.Наблюдатель это душа. Про пассивного никто не говорит. Душа активна.
Заповеди соблюдать Вам никто не мешает. А Библию каждый толкует как ему нравится. Библия не для буквального понимания. Это не книга научная, научных открытий по которую надо подгонять науку.Средневековье оклеветано врагами христианства. Возможно, не так там все было плохо. И наша задача не защитить существование Бога, Он в нашей защите не нуждается. Наша задача отстоять для нас и наших детей возможность жить по Заповедям, содержащимся в Священном Писании.
Священное Писание не содержит ошибок, которые приписывают ему эволюционисты. И заповеди святы.
А теорию эволюции и др. антибиблейские вещи продвигают те, кто хочет грешить и считаться при этом порядочным человеком.
Библия книга о Боге и душе.
- Православный христианин
2Тим.4:3: Ибо будет время, когда здравого учения принимать не будут, но по своим прихотям будут избирать себе учителей, которые льстили бы слуху.Заповеди соблюдать Вам никто не мешает. А Библию каждый толкует как ему нравится. Библия не для буквального понимания. Это не книга научная, научных открытий по которую надо подгонять науку.
Библия книга о Боге и душе.
А те, кто хотят спастись, толкуют Библию так, как научены Святые Отцы Духом Святым.
Хотя Библия и не относится к научной литературе, но там все истинно и нет никаких ошибок, чему постоянно находит подтверждения истинная наука. А эволюционисты хотят унизить авторитет Библии, чтобы заповеди подогнать под свои интересы.
- Православный христианин
«Христианский» эволюционизмТеория эволюции не отрицает Бога.
В связи с фундаментальной важностью креационизма для библейского христианства, о чем было сказано ... и мертвящего влияния эволюционной теории как социально-религиозной философии... , становится очевидным, что истинным христианам следует питать отвращение к эволюции и противостоять ей изо всех сил. Однако трагедия заключается в том, что большинство верующих христиан или идут на компромисс с эволюцией или безразличны к ее важной роли.
Так называемые христианские «либералы»... давно приняли эволюцию. Этого можно было ожидать, так как либеральные теологи также отвергают непогрешимость Библии.
И наконец, выступление христианской Церкви против эволюционной теории было, как правило, неэффективным со времен Дарвина. Конечно, были значительные исключения из правил, но эти отдельные исключения были недостаточными, чтобы остановить течение эволюционной мысли.
Подтверждено, что большинство эволюционистов не являются атеистическими гуманистами (хотя большинство представителей и лидеры эволюционной мысли кажутся таковыми). Типичная точка зрения мирянина на эволюцию заключается в том, что она как-то связана с методом творения Бога и поэтому не должна являться предметом особой заботы для христиан. Большое число «вновь рожденных» христиан признаются под давлением, что они «эволюционисты-теисты».
Однако креационисты давно считают, что теистическая эволюция — это такая же несуразица, как «христианский атеизм». Если эволюция может объяснить все формы жизни, как утверждают ведущие эволюционисты, тогда Бог излишен. Более того, сама суть эволюционизма — цепь случайностей, пустая, бессмысленная борьба за выживание. Сами эти термины несовместимы с мудростью и силой Бога и с этикой христианства. Однако эти соображения часто игнорируются, особенно когда на них указывают библейские фундаменталисты.
Поэтому вдвойне примечательно, когда на этот факт указывает ведущий научный эволюционист-атеист Жак Моно. В интервью по радио, данном в Австралии незадолго до своей смерти, выдающийся французский биолог, лауреат Нобелевской премии и автор влиятельной книги «Шанс и необходимость» заявил (по сообщению австралийского креационистского журнала «Экс нихило»), касаясь эволюционного процесса:
«Почему Богу пришлось выбрать такой чрезвычайно сложный и трудный механизм?.. Почему сразу же не создать человека, во что, разумеется, верит классическая религия?".
Моно, конечно, выбрал веру в полный натурализм и атеизм, принужденный к этому неумолимой логикой бесспорного, по его мнению, «факта» эволюции. Далее он сказал:
"[Естественный] отбор является самым слепым и жестоким способом возникновения новых видов… Борьба за жизнь и ликвидация слабейших — ужасный процесс, против которого восстает наша современная этика. Идеальное общество — это не прошедшее через систему отбора общество; общество, где слабый защищен, что прямо противоположно так называемому естественному закону. Я удивлен, что христианин может утверждать, что Бог в какой-то степени запустил этот процесс, чтобы иметь эволюцию».
Если уж атеист удивляется тому, что христианин может защищать эволюцию, то каким должно быть отношение Самого Бога к такой компромиссной точке зрения, которая не только отвергает ясное учение Слова Божия, но даже клевещет на Его Личность?
Я говорю про то, что согласно физике Вы Наблюдатель в данный момент времени и пространства.Я не думаю, что душа человеческая наблюдала, как Бог создает мир.
Про начало создание Вселенной речи не стоит, т.к. это миллиарды лет только видимой части. Есть научная теория что Вселенная циклична. Т.е. мир безначален. Не мог Бог бесконечное время созревать, чтобы однажды 10 тыс лет назад принять решение, что мол скучно, дай ка я создам творение.
Думать так, значит опуститься до человеческого уровня понимания. Это примитивное мышление.
Понятие тварное означает искаженное(греховное).
Душа может в любой момент времени уничтожить эту реальность тварного мира и войти в нетварный мир подлинной духовности.
Это православная аскетика. Я уже говорил что она не похожа на рациональную веру.
Этот тип мистических переживаний прикосновения к Непостижимой Великой Сущей Реальности, пред которой реальность этого мира уничтожается, — для христианина есть лишь начало подлинной духовной жизни.
http://litra.pro/pravoslavie---svideteljstvo-istini-iz-pisem-k-d-baljfuru/saharov-sofronij/read/11
/Архимандрит Софроний Сахаров О росте духовного сознания/
Когда душа выходит за пределы рассудочной деятельности и чувств человеческих в молитве высшего порядка, тогда и происходит восхождение на вершину духа к высшей реальности.
Вся наша условная реальность ощущается только физическими органами чувств и рассудком человеческим.
Кто это понимает, тот допускает и инопланетян, и другие Вселенные и что творение было всегда.
Последнее редактирование:
- Интересующийся
Валерий, я понимаю Ваше затруднение с ВНТ. Вы описываете только часть процессов наблюдаемых в природе, а именно те, которые ведут к возрастанию энтропии, но не видите тех процессов, которые приводят к временному локальному её снижению. Возможно, Вы просто не задумывались над этим, но взгляните внимательнее. Самоусложнение структур в неживой природе происходит без всякой генетической программы, почему это Вас не удивляет? Возьмите, например, ядерный синтез тяжёлых элементов (т.е. более сложных элементов) из более лёгких в недрах звёзд. Или гравитационное сепарирование - перемещение более тяжёлых элементов в центр планет, а более лёгких ближе к поверхности. Этот процесс делает из аморфной кучи веществ, к примеру, структурированную планету под названием Земля, с конвекционными процессами внутри, что в том числе разогревает её и приводит к вулканизму и образованию атмосферы и гидросферы. А тяжёлое железное ядро создаёт магнитное поле и т.д. Это Вам пример самоусложнения материи. И всё это из элементов, как правильно заметил Галиций, сформированных в недрах первых звёзд в результате процесса ядерного синтеза (так же самоусложнения материи). Вот Вам и процессы локального снижения энтропии без какой-либо программы.Вы что, издеваетесь? Если это ответ на вопрос о противоречии эволюции и второго закона термодинамики, то вы бредите. Эта цитата, которую вы скопировали неизвестно откуда вообще на этот вопрос не отвечает.
Если это даже открытая система, тогда в нее может поступать энергия извне. Но верить, что безликая энергия извне поможет создавать из хаоса порядок и из простых элементов более сложные то же самое, что верить, что ураган, пронесшийся над свалкой соберет из находящегося там мусора современный самолет.
Второй закон (Второе начало) термодинамики в самой общей форме звучит так: все физические системы, предоставленные самим себе, стремятся к дезорганизации, разрушению, беспорядку. Этот закон применим к любой системе, какой бы она ни была: и замкнутой, и открытой. Но для простоты математического выражения закона подразумевается, что в систему не поступает энергия и она является закрытой. Если в систему, в которой идут самопроизвольные процессы, поступает тепло, то ее стремление к хаосу и разупорядоченности только усилится и ускорится. Это хорошо иллюстрирует Третий закон термодинамики: наивысший порядок устанавливается при температуре абсолютного нуля (-273°С). Повышение температуры, то есть добавление энергии, разрушает этот порядок.
Любая природная система в реальности всегда открыта, то есть обменивается с внешней средой энергией и веществом. Тем не менее Вы прекрасно знаете, что все предоставленное самому себе приходит в негодность, изнашивается, ломается, рассыпается, распадается на части, ржавеет и т.д. Есть и другие аспекты Второго закона термодинамики, например, тепло самопроизвольно передается от горячего тела к холодному и никогда в обратном направлении. Иначе говоря, Вы постоянно наблюдаете неумолимое действие этого закона.
Что касается тезиса – действие Второго начала термодинамики не противоречит эволюции, то можно сказать однозначно: этот закон категорически запрещает самопроизвольное движение к более упорядоченному и сложноорганизованному состоянию материального мира.
Чтобы система перешла в более сложноорганизованное состояние, нужна информация (программа) для этого усложнения и энергия в той форме, которую может использовать данная система. Как и сама информация не создается в самопроизвольных, случайных процессах. Она появляется только из разумного источника. А просто энергия – неуправляемая и непреобразованная – способна лишь ускорить и усилить движение к распаду и хаосу. Эволюционисты же фантазируют, что солнечной энергии было достаточно для эволюционного движения вверх от молекулы к человеку. Живые организмы используют солнечную энергию только после ее преобразования, вначале в энергию химических связей органических веществ. Это осуществляют зеленые растения в фотосинтезе – сложнейшем процессе, информация о котором закодирована в растительной клетке. Живыми организмами энергия извлекается из органических веществ и запасается в виде энергии АТФ (аденозинтрифосфорной кислоты, энергетической валюты клетки). Это тоже сложнейший механизм, программа которого заложена в генетическом аппарате клетки.
Вот Вам еще одна иллюстрация. Сколько ни подавай солнечной энергии, даже в течение предполагаемого эволюционистами возраста Вселенной около 15 миллиардов лет, строительные материалы не превратятся в дом, а груда металла в автомобиль. Без проекта и чертежей (внесения информации), сознательного труда и использования управляемой энергии (бензин, электричество, мышечная работа и пр.) ни дом, ни автомобиль не создать. В самих строительных материалах и металле не содержится ничего, что могло бы породить созидательный процесс.
...Примеры по проведению уборки в жилище как раз свидетельствуют: чтобы повысить упорядоченность и организацию системы, необходим осмысленный труд, использование материально-энергетических ресурсов в нужном месте, в нужное время, в нужном количестве. Без этого начнет действовать Второй закон термодинамики. Жилье начнет припадать пылью, ветшать и разваливаться, даже если там никто не живет.
Если хотите, можете ещё вот этот материал прочитать:
Глава 4а. Термодинамические подходы к сущности жизни. Второе начало термодинамики, энтропия и диссипативные структуры
Здесь нам опять придется начать издалека. В 1847 году Г. Гельмгольц сформулировал закон сохранения энергии (ЗСЭ). Следует помнить, что ЗСЭ является всего лишь эмпирическим обобщением: вообще говоря, никто не знает, почему энергию нельзя ни сотворить из ничего, ни уничтожить - просто этого не происходит ни в каких, сколь угодно хитроумных, наблюдениях и экспериментах. Мы с вами помним, что однажды ЗСЭ основательно пошатнулся - когда возникла необходимость объяснить, отчего светит Солнце (см. главу 1), однако тут подоспело открытие Эйнштейном эквивалентности массы и энергии, и все опять встало на свои места. Именно поэтому ни одно патентное бюро не станет рассматривать проект устройства для получения большей энергии, чем оно потребляет; такое устройство получило название вечный двигатель первого рода.
Первой созданной человеком машиной для превращения тепла в механическую энергию был паровой двигатель. Это устройство производит работу путем перемещения энергии в форме тепла из горячего резервуара (с паром) в холодный резервуар (с водой). Поэтому раздел физики, занимающийся взаимными превращениями работы и энергии, назвали термодинамикой, а паровой двигатель очень долго оставался его основной моделью. Первое начало термодинамики гласит, что "если резервуар с паром содержит некоторое количество энергии, то от паровой машины нельзя получить больше работы, чем допускает запас этой энергии". Легко видеть, что оно является одной из формулировок ЗСЭ; именно первое начало термодинамики и нарушает "вечный двигатель первого рода".
Ну, ладно: нельзя так нельзя. Но уж по крайней мере всю работу, что содержится в паре, мы можем извлечь? Имеется в виду - если полностью устранить трение и всякие иные потери? Увы - оказывается, нет. Даже в идеальном случае не то что выиграть - нельзя даже "получить свое". В 1824 году С. Карно установил, что доля тепловой энергии, которая может быть (даже в идеале!) превращена в работу, зависит от разности температур горячего и холодного резервуаров.
Идеальная отдача K = (Т2-Т1)/Т2, где Т1 и Т2 - температура холодного и горячего резервуаров (в градусах абсолютной шкалы Кельвина). Пусть, например, Т2 будет 400о (=127оС), а Т1 300о (=27оС). В этом случае K = (400-300)/400=0,25. То есть - даже в этом идеализированном случае лишь четверть энергии сможет быть превращена в работу, а остальные три четверти - бесполезно пропадут.
Если же у нас имеется только один резервуар (он же горячий, он же и холодный), то идеальная отдача, соответственно, будет равна нулю. То есть - энергии-то в этом резервуаре с паром сколько угодно, но ни единая часть ее не может быть превращена в работу. Все это полностью относится и к другим видам энергии: работа, которую может совершить камень, падающий с края обрыва, зависит от высоты последнего (т.е. от разности потенциальных энергий камня), однако камень, лежащий посреди плоскогорья на высоте 5 километров, никакой работы совершить не может. В этом и состоит одна из формулировок Второго начала термодинамики (ВНТ): "ни одно устройство не может извлечь работу из системы, которая целиком находится на одном потенциальном уровне".
Устройство, предназначенное для извлечения работы из системы, имеющей единственный энергетический уровень (и, соответственно, нарушающее ВНТ), называется вечным двигателем второго рода. Представляете, как было бы здорово - откачать, например, энергию теплового движения молекул кастрюльки с водой (кастрюлька-то пускай при этом замерзнет - закон сохранения энергии мы чтим!) и перевести ее в механическую, электрическую, или еще какую-нибудь путную форму. Только ничего из этой затеи не выйдет - вечный двигатель второго рода невозможен точно так же, как и первого.
Между тем, как только в системе появляются два энергетических уровня, энергия тут же начинает перетекать от более высокого уровня к низкому: тепло переходит от горячего тела к холодному, камень падает с обрыва, ток начинает течь от анода к катоду, и т.д. (поэтому существует и другая формулировка ВНТ: "Поток энергии всегда направлен от высокого потенциального уровня к низкому"). В случае, если наша паровая машина представляет собой замкнутую систему (т.е. никакое вещество и энергия не могут ни проникнуть в нее извне, ни покинуть ее), горячий резервуар будет постепенно остывать, а холодный - нагреваться; то есть - в течении всего времени, пока в системе совершается работа разность температур резервуаров будет неуклонно падать. Тогда, в соответствии с соотношением Карно, доля содержащейся в системе энергии, которую можно обратить в работу, будет уменьшаться, а доля той "омертвленной" энергии, что недоступна для такого превращения - необратимо расти. Поэтому ВНТ может быть сформулировано еще и так: "В любом самопроизвольном процессе (когда энергии открыт путь для перетекания с более высокого уровня на низкий) количество недоступной энергии со временем увеличивается".
В 1865 году Р. Клаузиус, имея дело с этой самой необратимо теряемой (диссипированной) энергией, ввел специальную величину, названную им энтропией (S); она отражает отношение тепловой энергии к температуре и имеет размерность кал/град. В любом процессе, связанном с превращениями энергии, энтропия возрастает или - в идеальном случае (горячий и холодный резервуары разделены абсолютным теплоизолятором, ток течет по сверхпроводнику и т.д.) - не уменьшается. Поэтому ВНТ иногда называют Законом неубывания энтропии. А самая краткая объединенная формулировка первого и второго начал термодинамики, предложенная тем же Клаузиусом (1865), звучит так: В любой замкнутой системе полная энергия остается постоянной, а полная энтропия с течением времени возрастает.
Пусть у нас есть та же самая пара резервуаров - горячий и холодный; их соединяют, в результате чего их температуры (отражающие среднюю кинетическую энергию молекул) уравниваются. Можно описать эту картину и так: "Система вначале была структурирована - поделена на горячую и холодную части, а затем эта структура разрушилась; система перешла из упорядоченного состояния в беспорядочное, хаотическое". Понятиям "порядок" и "хаос" не так-то просто дать строгие определения, однако интуитивно мы подразумеваем, что порядок - это когда предметы разложены в соответствии с некой логической системой, а хаос - когда никакой системы не обнаруживается. Итак, мы видим, что когда энергия (в данном случае - тепловая) перетекает в направлении, указанном ВНТ, хаос (беспорядок) в системе возрастает. А поскольку энтропия при этом растет тоже, то возникает вполне логичное предположение: а не являются ли "хаос" и "энтропия" родственными, взаимосвязанными понятиями? Так оно и есть: в 1872 году Л. Больцман строго доказал, что Клаузиусова энтропия (S) действительно является мерой неупорядоченности состояния системы: S = k ln P, где k - универсальная постоянная Больцмана (3,29*10-24кал/гр), а P - количественное выражение неупорядоченности (оно определяется довольно сложным способом, который для нас сейчас неважен). Это соотношение называют принципом порядка Больцмана; оно означает, что необратимые термодинамические изменения системы всегда идут в сторону более вероятных ее состояний, и в конечном счете ведут к состоянию хаоса - максимальной выравненности и симметрии.
Поскольку в любой замкнутой системе энтропия непрерывно и необратимо возрастает, то со временем в такой системе, как наша Вселенная, исчезнет всякая структурированность и должен воцариться хаос. В частности, установится единая температура (которая, соответственно, будет лишь немногим выше абсолютного нуля). Эту гипотетическую ситуацию назвывают "тепловой смертью Вселенной"; рассуждения на эту тему были очень модны в конце прошлого века. Надо сказать, что закон неубывания энтропии - со всеми его глобально-пессимистическими следствиями - вообще создает массу неудобств для мироощущения любого нормального человека. Неудивительно, что регулярно возникает вопрос - а нельзя ли найти способ как-нибудь объегорить ВНТ и победить возрастание энтропии?
Те из вас, кто читал "Понедельник начинается в субботу", возможно, помнят работавших в НИИЧАВО вахтерами демонов Максвелла; кое-кто, возможно, даже прочел в "Словаре-приложении" разъяснение Стругацких, что существа эти были первоначально созданы "для вероломного нападения на Второе начало термодинамики". Суть мысленного эксперимента, осуществленного Дж. Максвеллом (1860) заключается в следующем. Есть два сосуда с газом, соединенные трубкой; система находится в тепловом равновесии - усредненные энергии молекул любых двух порций газа равны между собой. Это вовсе не означает, что все молекулы одинаковые: среди них есть более быстрые ("горячие") и более медленные ("холодные"), просто на больших числах это все усредняется. А что, если несколько быстрых молекул - чисто случайно! - перейдут из правого резервуара в левый, а несколько медленных - из левого в правый? Тогда левый сосуд несколько нагреется, а правый охладится (при этом суммарная энергия системы останется неизменной); в системе возникнет разность потенциалов, то есть - возрастет упорядоченность, а энтропия снизится. В реальности такие отклонения будут - по теории вероятностей - сугубо временными. Давайте, однако вообразим, что в соединяющей сосуды трубке сидит крошечный демон, который будет пропускать быстрые молекулы только слева направо, а медленные - справа налево. Через некоторое время все быстрые молекулы соберутся в правом сосуде, а все медленные - в левом, левый сосуд нагреется, а правый - охладится; значит, энтропия отступила. Понятное дело, что такого демона в действительности не существует, но может быть мы со временем сумеем создать некое устройство, работающее на этих принципах?
К сожалению, не сумеем. (Кстати, сам Максвелл и не думал покушаться на ВНТ: ему-то демон был нужен просто для объяснения температуры через скорость движения молекул - в противовес тогдашним представлениям о "невидимой жидкости-теплороде".) Все дело в том, что наши резервуары с газом не являются полной системой: полная же система состоит из газа плюс демона. "Отлавливая" молекулы с соответствующими параметрами, наш демон вынужден будет пахать как трактор. Поэтому повышение собственной энтропии демона с лихвой перекроет то понижение энтропии, которое он произведет в газе. Одним словом, мы имеем дело с классическим вечным двигателем второго рода.
Однако постойте: энтропию газа-то демон, как ни крути, понизил... А ведь это идея!.. Пускай суммарная энтропия некой системы (скажем, Вселенной) необратимо возрастает - ну и Бог с ней. Мы же займемся тем, что будем локально понижать энтропию и повышать упорядоченность - настолько, насколько нам нужно. Конечно, в других частях системы энтропия при этом вырастет, но нам-то что за дело? Реализуем ли такой сценарий? Разумеется - ведь саму жизнь вполне можно рассматривать как пример такого локального нарушения закона неубывания энтропии. Основатель квантовой механики Э. Шредингер в своей замечательной книге "Что такое жизнь с точки зрения физика?" именно так и определяет ее - как работу специальным образом организованной системы по понижению собственной энтропии за счет повышения энтропии окружающей среды.
Этот подход стал достаточно традиционным, однако он таит в себе ряд подводных камней - не научного, правда, а скорее философского плана. В рамках такого взгляда на проблему энтропия (вполне заурядная физическая величина) незаметно приобретает отчетливые черты некого Мирового Зла, а нормальное функционирование живых систем вдруг разрастается до масштабов глобального противостояния сил Света и Тьмы. (Следует заметить, что оные живые системы выглядят при этом отнюдь не толкиеновскими рыцарями, обороняющими Пеленорские поля от воинства Черного Властелина, а перепуганным мальчишкой, который безнадежно отчерпывает ржавой консервной банкой протекающую изо всех щелей лодку.) Поэтому нет ничего удивительного в том, что некоторые ученые на полном серьезе считают Второе начало термодинамики физическим воплощением Дьявола. Ну а раз есть Дьявол, то возникает необходимость для равновесия ввести в картину Мира и Бога (как некое антиэнтропийное, организующее начало); с этого самого момента весь этот комплекс проблем, строго говоря, изымается из сферы науки и переходит в сферу богословия. В любом случае, жизнь в своем противостоянии закону неубывания энтропии выглядит обреченной на сугубо оборонительную стратегию, что исключает повышение сложности ее организации. В рамках такого подхода дилемма, сформулированная Р. Кэллуа (1973) - "Могут ли и Карно, и Дарвин быть правы?" действительно кажется не имеющей решения.
Здесь необходимо подчеркнуть одно фундаментальное различие между термодинамикой (связанной "кровным родством" с химией) с одной стороны, и всей прочей физикой (выросшей, так или иначе, из классической механики) с другой. В классической динамике все процессы является обратимыми (это формулировали в явном виде все ее основатели, например, Галилей и Гюйгенс), а картина мира - детерминистической: если некое существо ("демон Лапласа") будет знать все параметры состояния Вселенной в некий момент времени, то оно сможет и точно предсказать ее будущее, и до мельчайших деталей реконструировать прошлое. Из обратимости же физических процессов следует, что время не является объективной реальностью, а вводится нами лишь для собственного удобства - как нумерация порядка событий: планеты могут обращаться вокруг Солнца как вперед, так и назад по времени, ничего не изменяя в самих основах ньютоновской системы. Революция, произведенная в физике Эйнштейном, этой сферы не затронула, а его окончательное суждение на сей предмет гласит: "Время (как и необратимость) - не более чем иллюзия". Случайности также не нашлось места в той картине Мира, что создана Эйнштейном; широко известна его чеканная формулировка - "Бог не играет в кости (God casts the die, not the dice)". Даже квантовая механика, наиболее отличная по своей "идеологии" от всех прочих физических дисциплин, сохраняет этот взгляд на проблему времени: в лежащем в ее основе уравнении Шредингера время остается однозначно обратимым.
Принципиально иную картину Мира рисовала термодинамика: здесь аналогом Вселенной являлся не часовой механизм с бесконечным заводом, а паровой двигатель, в топке которого безвозвратно сгорает топливо. Согласно ВНТ, эта мировая машина постепенно сбавляет обороты, неотвратимо приближаясь к тепловой смерти, а потому ни один момент времени не тождественен предыдущему. События в целом невоспроизводимы, а это означает, что время обладает направленностью, или, согласно выражению А. Эддингтона, существует стрела времени. Осознание принципиального различия между двумя типами процессов - обратимыми, не зависящими от направления времени, и необратимыми, зависящими от него - составляет саму основу термодинамики. Понятие энтропии для того и было введено, чтобы отличать первые от вторых: энтропия возрастает только в результате необратимых процессов. При этом, как заключает И. Пригожин, "стрела времени" проявляет себя лишь в сочетании со случайностью: только если система ведет себя достаточно случайным образом, в ее описании возникает реальное различие между прошлым и будущим, и, следовательно, необратимость. Картина Мира становится стохастической - то есть точно предсказать изменения Мира во времени принципиально невозможно, а потому демона Лапласа следует отправить в отставку за полной его бесполезностью.
В XIX веке изучали лишь наиболее простые, замкнутые системы, не обменивающиеся с внешней средой ни веществом, ни энергией; при этом в центре внимания находилась конечная стадия термодинамических процессов, когда система пребывает в состоянии, близком к равновесию. Тогдашняя термодинамика была равновесной термодинамикой. Именно равновесные состояния (в разреженном газе) изучал Больцман, с чем и была связана постигшая его творческая неудача: горячо восприняв идею эволюции (хорошо известна его оценка: "Девятнадцатый век - это век Дарвина"), он потратил массу сил и времени на то, чтобы дать дарвинизму строгое физическое обоснование - но так и не сумел этого сделать [11]. Более того, введенный им принцип порядка налагает прямой запрет на возникновение организованных (и потому менее вероятных) структур из неорганизованных - т.е. на прогрессивную эволюцию. На неравновесные же процессы в то время смотрели как на исключения, второстепенные детали, не заслуживающие специального изучения.
Ныне ситуация коренным образом изменилась, и как раз замкнутые системы теперь рассматривают как сравнительно редкие исключения из правила. При этом было установлено, что в тех открытых системах, что находятся в сильно неравновесных условиях, могут спонтанно возникать такие типы структур, которые способны к самоорганизации, т.е. к переходу от беспорядка, "теплового хаоса", к упорядоченным состояниям. Создатель новой, неравновесной термодинамики Пригожин назвал эти структуры диссипативными - стремясь подчеркнуть парадокс: процесс диссипации (т.е. безвозвратных потерь энергии) играет в их возникновении конструктивную роль. Особое значение в этих процессах имеют флуктуации - случайные отклонения некой величины, характеризующей систему из большого числа единиц, от ее среднего значения (одна из книг Пригожина так и называется - "Самоорганизация в неравновесных системах. От диссипативных структур к упорядочению через флуктуации").
Одним из простейших случаев такой спонтанной самоорганизации является так называемая неустойчивость Бенара. Если мы будем постепенно нагревать снизу не слишком толстый слой вязкой жидкости, то до определенного момента отвод тепла от нижнего слоя жидкости к верхнему обеспечивается одной лишь теплопроводностью, без конвекции. Однако когда разница температур нижнего и верхнего слоев достигает некоторого порогового значения, система выходит из равновесия и происходит поразительная вещь. В нашей жидкости возникает конвекция, при которой ансамбли из миллионов молекул внезапно, как по команде, приходят в согласованное движение, образуя конвективные ячейки в форме правильных шестиугольников. Это означает, что большинство молекул начинают двигаться с почти одинаковыми скоростями, что противоречит и положениям молекулярно-кинетической теории, и принципу порядка Больцмана из классической термодинамики. Если в классической термодинамике тепловой поток считается источником потерь (диссипации), то в ячейках Бенара он становится источником порядка. Пригожин характеризует возникшую ситуацию как гигантскую флуктуацию, стабилизируемую путем обмена энергией с внешним миром.
Еще более удивительны явления самоорганизации, происходящие в неравновесных химических системах (например, в так называемых химических часах). Если в ячейках Бенара речь шла о согласованных механических движениях молекул, то здесь мы имеем дело со столь же согласованными, "как по команде", их химическими превращениями. Предположим, что у нас имеется сосуд с молекулами двух сортов - "синими" и "красными". Движение молекул хаотично, поэтому в любой из частей сосуда концентрация "синих" и "красных" молекул будет несколько отклоняться от средней то в одну, то в другую сторону, а общий цвет реакционной смеси должен быть фиолетовым с бесконечными переходами в сторону синего и красного. А вот в химических часах мы увидим нечто совершенно иное: цвет всей реакционной смеси будет чисто-синий, затем он резко изменится на чисто-красный, потом опять на синий, и т.д. Как отмечает Пригожин, "столь высокая упорядоченность, основанная на согласованном поведении миллиардов молекул, кажется неправдоподобной, и если бы химические часы нельзя было наблюдать "во плоти", вряд ли кто-нибудь поверил бы, что такой процесс возможен". (По поводу последнего следует заметить, что первооткрывателю этого типа реакций П.Б. Белоусову пришлось на протяжении многих лет доказывать, что демонстрируемые им - причем именно "во плоти"! - химические часы не являются просто фокусом.) Помимо химических часов, в неравновесных химических системах могут наблюдаться и иные формы самоорганизации: устойчивая пространственная дифференциация (в нашем примере это означало бы, что правая половина сосуда окрасится в красный цвет, а левая - в синий), или макроскопические волны химической активности (красные и синие узоры, пробегающие по фиолетовому фону).
Однако для того, чтобы в некой системе начались процессы самоорганизации, она должна быть как минимум выведена из стабильного, равновесного состояния. В ячейках Бенара неустойчивость имеет простое механическое происхождение. Нижний слой жидкости в результате нагрева становится все менее плотным и центр тяжести смещается все дальше наверх; по достижении же критической точки система "опрокидывается" и возникает конвекция. В химических системах ситуация сложнее. Здесь стационарное состояние системы представляет собой ту стадию ее развития, когда прямая и обратная химические реакции взаимно уравновешиваются, и изменения концентрации реагентов прекращаются. Вывести систему из этого состояния очень трудно, а в большинстве случаев - просто невозможно; не зря реакции типа "химических часов" были открыты лишь недавно, в пятидесятые годы (хотя их существование было теоретически предсказано математиком Р. Вольтерра еще в 1910 г.). Для того, чтобы устойчивость стационарного состояния оказалась нарушенной, есть одно необходимое (но не достаточное) условие: в цепи химических реакций, происходящих в системе, должны присутствовать автокаталитические циклы, т.е. такие стадии, в которых продукт реакции катализирует синтез самого себя. А ведь именно автокаталитические процессы, как мы помним по Главе 4, составляют основу такого процесса, как жизнь.
Итак, жизнь можно рассматривать как частный случай в ряду процессов химической самоорганизации в неравновесных условиях, происходящих на основе автокатализа. Интересно, однако, при этом сопоставить функционирование живых объектов и самоорганизующихся неорганических систем. В примерах самоорганизации, известных из неорганической химии, участвующие в реакциях молекулы просты, тогда как механизмы реакций сложны. Например, в реакции Белоусова-Жаботинского (окисление малоновой кислоты броматом калия, катализируемое солями церия) насчитывается около тридцати промежуточных продуктов. В примерах же самоорганизации, известных из биологии, схема реакции, как правило, проста, тогда как участвующие в ней молекулы (белки, нуклеиновые кислоты) очень сложны и специфичны. Это различие представляется Пригожину чрезвычайно важным, соответствующим фундаментальному различию между биологией и физикой: "У биологических систем [в отличие от физических - К.Е.] есть прошлое. Образующие их молекулы - итог предшествующей эволюции, они были отобраны для участия в автокаталитических механизмах". Этот вывод впрямую перекликается с известными нам по Главе 4 построениями М. Эйгена о самоорганизации молекул на основе матричной репродукции и естественного отбора.
Думаю, не будет ошибкой сказать, что бурно развивающаяся неравновесная термодинамика буквально на наших глазах меняет всю картину Мира, в котором мы живем. Например, второе начало термодинамики приобретает в ней совершенно иной философский смысл, ибо именно энтропия является тем самым "сырьем", из которого диссипативные структуры могут создать (а могут и не создать - это дело случая!) более высокую, чем прежде, упорядоченность. Для нас же здесь наиболее существенно то, что в ее рамках процесс происхождения жизни теряет свою абсолютную уникальность (а вместе с нею - и сопутствующий мистический ореол) и становится обычной, хотя и чрезвычайно сложной, научной проблемой. Как пишет Пригожин, "старая проблема происхождения жизни предстает в новом свете. Заведомо ясно, что жизнь несовместима с принципом порядка Больцмана, но не противоречит тому типу поведения, который устанавливается в сильно неравновесных условиях", и далее: "Разумеется, проблема происхождения жизни по-прежнему остается весьма трудной, и мы не ожидаем в ближайшем будущем сколько-нибудь простого ее решения. Тем не менее, при нашем подходе жизнь перестает противостоять "обычным" законам физики, бороться против них, чтобы избежать предуготованной ей судьбы - гибели."
Примечания
11. Стоявшую перед Больцманом проблему в 1983 году удалось решить Ю. Л. Климонтовичу, строго доказавшему возможность уменьшения энтропии в процессе самоорганизации – но только для открытых систем. S-теорема Климонтовича является аналогом существующей для закрытых систем H-теоремы Больцмана, гласящей, что энтропия системы монотонно возрастает и остается неизменной при достижении равновесного состояния.
Кирилл Еськов "Удивительная палеонтология"
Последнее редактирование:
- Православный христианин
Мы можем о Боге знать наверняка только то, что Он Сам о Себе открыл. Все остальное - фантазии и предположения.Я говорю про то, что согласно физике Вы Наблюдатель в данный момент времени и пространства.
Про начало создание Вселенной речи не стоит, т.к. это миллиарды лет только видимой части. Есть научная теория что Вселенная циклична. Т.е. мир безначален. Не мог Бог бесконечное время созревать, чтобы однажды 10 тыс лет назад принять решение, что мол скучно, дай ка я создам творение.
Думать так, значит опуститься до человеческого уровня понимания. Это примитивное мышление.
Понятие тварное означает искаженное(греховное).
Душа может в любой момент времени уничтожить эту реальность тварного мира и войти в нетварный мир подлинной духовности.
Это православная аскетика. Я уже говорил что она не похожа на рациональную веру.
Этот тип мистических переживаний прикосновения к Непостижимой Великой Сущей Реальности, пред которой реальность этого мира уничтожается, — для христианина есть лишь начало подлинной духовной жизни.
http://litra.pro/pravoslavie---svideteljstvo-istini-iz-pisem-k-d-baljfuru/saharov-sofronij/read/11
/Архимандрит Софроний Сахаров О росте духовного сознания/
Когда душа выходит за пределы рассудочной деятельности и чувств человеческих в молитве высшего порядка, тогда и происходит восхождение на вершину духа к высшей реальности.
Вся наша условная реальность ощущается только физическими органами чувств и рассудком человеческим.
Кто это понимает, тот допускает и инопланетян, и другие Вселенные и что творение было всегда.
- Православный христианин
По вашему получается, что ядерная реакция, основанная на слиянии протонов и нейтронов - это движение от менее упорядоченной системы к более упорядоченной?Валерий, я понимаю Ваше затруднение с ВНТ. Вы описываете только часть процессов наблюдаемых в природе, а именно те, которые ведут к возрастанию энтропии, но не видите тех процессов, которые приводят к временному локальному её снижению. Возможно, Вы просто не задумывались на этим, но взгляните внимательнее. Самоусложнение структур в неживой природе происходит без всякой генетической программы, почему это Вас не удивляет? Возьмите, например, ядерный синтез тяжёлых элементов (т.е. более сложных элементов) из более лёгких в недрах звёзд. Или гравитационное перемещение более тяжёлых элементов в центр планет, а более лёгких ближе к поверхности. Этот процесс делает из аморфной кучи веществ, к примеру, структурированную планету под названием Земля. С конвекционными процессами внутри, что в том числе разогревает её и приводит к вулканизму и образованию атмосферы и гидросферы. А тяжёлое железное ядро создаёт магнитное поле и т.д. Это Вам пример самоусложнения материи. И всё это из веществ, сформированных в недрах первых звёзд в результате процесса ядерного синтеза (так же самоусложнения материи). Вот Вам и процессы локального снижения энтропии без какой-либо программы.
Тут просто действуют законы природы, созданные Творцом. Программа для таких элементарных действий не нужна. Достаточно законов природы и свойств веществ.
Реакция, осуществимая при наиболее низкой температуре — дейтерий + тритий[5]:

Два ядра: дейтерия и трития сливаются, с образованием ядра гелия (альфа-частица) и высокоэнергетического нейтрона.
Да, образуется другое ядро путем слияния 1+1=2.
И что же? Это разве самоорганизация материи?
При горении тоже образуются другие вещества. Формула горения метана:

Образовались углекислый газ и вода.
Не понимаю, как формулы взаимодействия веществ доказывают теорию эволюции. И как это свидетельствует о снижении энтропии?
Закон всемирного тяготения создал Бог. Но если метеорит упадет на землю, то неужели это можно расценивать как самоорганизацию материи от простого к сложному? Даже если 2 планеты столкнуться это не будет чем-то более сложным. Это просто действие закона притяжения, созданного Творцом.
Последнее редактирование:
- Православный христианин
- Православный христианин
В конце вашей ссылки, Димитрий, есть цитата: "Как пишет Пригожин, "старая проблема происхождения жизни предстает в новом свете. Заведомо ясно, что жизнь несовместима с принципом порядка Больцмана, но не противоречит тому типу поведения, который устанавливается в сильно неравновесных условиях", и далее: "Разумеется, проблема происхождения жизни по-прежнему остается весьма трудной, и мы не ожидаем в ближайшем будущем сколько-нибудь простого ее решения. Тем не менее, при нашем подходе жизнь перестает противостоять "обычным" законам физики, бороться против них, чтобы избежать предуготованной ей судьбы - гибели."
Это говорит о том, что у науки нет доказательств эволюционного происхождения жизни. Что и требовалось доказать.
Это говорит о том, что у науки нет доказательств эволюционного происхождения жизни. Что и требовалось доказать.
- Православный христианин
Исключительная слабость, заключающаяся в фактически полном отсутствии каких-либо научных свидетельств естественного происхождения жизни где-то во Вселенной — это тщательно сохраняемый секрет нашей официальной науки, образования и средств массовой информации.
У верующих может не хватить знаний, чтобы разоблачить хитроумные наукообразные фокусы эволюционистов или написанные тяжелым научным слэнгом нечестные объяснения. Но когда эволюционисты имеют дело с подготовленными учеными-креационистами, они разводят руками и вынуждены признаться, что научных доказательств эволюционной теории нет.
У верующих может не хватить знаний, чтобы разоблачить хитроумные наукообразные фокусы эволюционистов или написанные тяжелым научным слэнгом нечестные объяснения. Но когда эволюционисты имеют дело с подготовленными учеными-креационистами, они разводят руками и вынуждены признаться, что научных доказательств эволюционной теории нет.
- Интересующийся
Именно так Валерий 1+1+1+1... и т.д., а что же это как не усложнение? Далее из новых элементов синтезируются ещё более сложные, вплоть до железа. Да, именно под действием простых законов природы идёт дальнейшее усложнение. Когда звёзды взрываются и выбрасывают более сложные элементы, чем водород и гелий, то из этих элементов образуются более сложные неорганические соединения, из которых в свою очередь синтезируются простые органические молекулы.По вашему получается, что ядерная реакция, основанная на слиянии протонов и нейтронов - это движение от менее упорядоченной системы к более упорядоченной?
Почитайте про опыты Миллера-Юри - (только не воспринимайте этот опыт как правильную реконструкцию древней атмосферы - это не так, с 1953г данные были уточнены и эксперименты скорректированы и получены ещё более потрясающие результаты), - где брались простые неорганические вещества, такие как СО2,NH3,CH4,H20. И под действием нагревания и электрических разрядов, через определённое время, синтезировались (без всякой программы) аминокислоты! Правда, аминокислоты в таких условиях получаются не чистыми хирально (количество правых и левых изомеров было равным), а как известно природные белки состоят только из левозакрученных аминокислот, а РНК и ДНК из правозакрученных нуклеотидов. Так вот, эта трудность (получение хирально чистых растворов) казалась долгое время непреодолимой для неживой природы. Креационисты трубили об этом постоянно. И действительно - это был сильный аргумент против абиогенеза. Но вот относительно недавно учёные обнаружили в природе естественный процесс отбора хирально чистых молекул нуклеотидов и аминокислот на минеральной подложке! Сама микроструктура простых минералов отбирет молекулы с определённой хиральностью. И это благодаря всё тем же простым природным законам!
И в области абиогенеза за последние полтора десятка лет наступил поистине прорыв. Сейчас уже не стоит вопрос о возможности или невозможности появления первой самокопирующейся молекулы РНК/ДНК или клетки, а вопрос стоит каким из нескольких десятков открытых способов это произошло. Далеко не вся картина ясна и возможно никогда на 100% открыта не будет, но уже сейчас учёные определили с большой степенью точности в каких условиях и при каких последовательных процессах самозарождалась жизнь. Конечно, эта сфера не столь разработана и проверена как дальнейшая эволюция самокопирующихся организмов, но бОльшая доля чудесности и невероятности с абиогенеза уже снята.
Вы всё время представляете действие природных процессов, к коим относятся и эволюционные, как некий чудесный "скачёк в сложности", хотя на самом деле всё происходит постепенно - от простого к сложному, как в недрах горящей звезды. И в этом нет ничего мистического, в отличии от идеи создания жизни из ничего путём творения, неким Творцом, и неким непонятным способом. Идея самоорганизации материи гораздо проще и нагляднее, её мы наблюдаем постоянно вокруг нас в живой и неживой природе, а вот процесс творения из ничего сложной биологической жизни мы нигде не видим.
Хорошую аналогию приводил Докинз для сравнения эволюции и божественного творения. Если представить сложную биологическую форму жизни как кодовый замок с двадцатизначным кодом, то божественное творение - это как правильный набор этого кода с первого раза, случайно его набрать практически невозможно, нужно его знать. А эволюция - это постепенный, медленный взлом каждой позиции в двадцатизначном коде путём перебора цифр сначала в первой позиции, после получения правильной цифры взлом второй позиции и т.д (и этот процесс мы наблюдаем в экспериментах). Да, такой процесс долог, но он отличается и от введения сразу правильного кода, и от перебора всех возможных вариантов случайным образом. Алгоритм этого способа вскрыть код (т.е. достичь современной сложности биологической жизни) - это сочетание случайных мутаций и отбора по определённым правилам, основанным на простых природных законах!
- Интересующийся
Валерий, креационисты Вас и тут ввели в заблуждение. Вот Вам прекрасный пример полезных мутаций, и это всё на наших глазах.Сейчас наукой доказано, что мутаций полезных не бывает (см. К. Виланд "Камни и кости"). Все мутации - это генетические ошибки, ведущие к инвалидизации особей и резком уменьшении их шансов на выживание (а на рождение потомства и подавно). Т.е. накопление генетических ошибок и мутаций - это не эволюция, это энтропия.
Александр Марков "Эволюция"
Глава 4. Эволюция на наших глазах
Часто для того, чтобы принять факт, нам нужно его увидеть. Факт эволюции некоторым людям принять непросто именно потому, что увидеть эволюцию воочию очень трудно. Ведь по меркам человеческой жизни эволюция – чудовищно медленный процесс. Как правило, для того, чтобы эволюционные изменения стали заметны, нужно ждать сотни тысяч, а то и миллионы лет. Две изолированные популяции должны оставаться изолированными примерно 3 млн лет, чтобы полностью утратить репродуктивную совместимость (способность производить плодовитое гибридное потомство). Но это в среднем. К счастью для нас (биологов, изучающих эволюцию), ее темпы крайне неравномерны. Некоторые виды – так называемые живые ископаемые – могут оставаться почти неизменными десятки и даже сотни миллионов лет, зато другие демонстрируют настолько быстрые изменения, что их вполне можно заметить даже на протяжении одной-единственной человеческой жизни. В лаборатории, подобрав подходящие условия, можно заставить некоторые организмы эволюционировать еще быстрее, так что даже появляется шанс получить интересные результаты всего за несколько лет работы. Поэтому эволюционные эксперименты в лаборатории важны и с точки зрения понимания эволюционных механизмов, и с точки зрения восприятия самого факта эволюции.
Для таких экспериментов нужно тщательно выбирать подходящие лабораторные объекты и знать, куда смотреть. Последнее зависит от того, какие именно эволюционные события мы надеемся увидеть. Конечно, не превращение мухи в слона[48]. Обычно экспериментаторы надеются увидеть любую наследуемую адаптацию к окружающим условиям, дающую выигрыш в эффективности размножения. Если на наших глазах объект сумел адаптироваться к предложенным условиям и передал новые свойства потомкам, значит, мы увидели самую настоящую эволюцию. Осталось разобраться, как именно он это сделал, какие получил мутации.
Никто, конечно, не проводит эволюционные эксперименты на баобабах и слонах. Любому исследователю хочется дожить до результатов своего опыта. А ведь нужно еще ежегодно отчитываться перед работодателями, иначе вас выгонят с работы или не продлят финансирование по гранту. «Баобабы на нашей плантации подросли еще на полметра, лет через 50 надеемся получить первые семена» – за такой годовой отчет вас по головке не погладят. Но вот, например, бактерии, у которых смена поколений происходит несколько раз в сутки, – превосходный объект для эволюционных экспериментов. Годятся дрожжи Saccharomyces cerevisiae, круглые черви C. elegans, насекомые, растения с коротким жизненным циклом, аквариумные рыбки, шпорцевые лягушки и другие быстро плодящиеся существа. Но с бактериями работать проще всего, и не только из-за рекордной скорости смены поколений. Немаловажно и то, что многомиллионная популяция запросто помещается в одной колбе.
В этой главе мы разберем, какие эволюционные процессы можно наблюдать своими глазами в лаборатории или в природе. Такие наблюдения подобны процессу препарирования: разрезая лягушку, примерно знаешь, что там будет внутри, но детали строения всегда неожиданны и информативны.
Приспособленность меняется постепенно
Начнем с самого масштабного и самого известного эволюционного эксперимента. В 1988 году группа биологов из Университета штата Мичиган под руководством Ричарда Ленски начала – и продолжает по сей день – уникальный эксперимент на бактериях, который позволил с небывалой доселе детальностью проследить ход эволюции как на уровне генома (накопление мутаций), так и на уровне целого организма (развитие адаптаций).
Эксперимент проводится параллельно с 12 популяциями кишечной палочки Escherichia coli. Эта бактерия – обычный обитатель кишечника теплокровных животных, включая человека. Все 12 подопытных популяций живут в аэробных условиях[49] в жидкой прозрачной среде, где единственной пищей является глюкоза. Именно количество глюкозы является лимитирующим фактором, ограничивающим размножение микробов. С интервалом в сутки из каждой популяции берут небольшую часть (0,1 мл содержимого колбы) и пересаживают в новую колбу с 9,9 мл свежей питательной среды. Там бактерии быстро размножаются, пока не исчерпают запасы глюкозы. Таким образом, в течение каждого суточного цикла начальный период изобилия, когда численность популяции быстро растет, сменяется периодом голода, когда бактерии перестают размножаться и их численность стабилизируется. Численность бактерий оценивают по мутности среды – обычный и весьма надежный метод при наличии соответствующего оборудования.
Периодически часть каждой популяции замораживают при −80 °C (что ничуть не вредит здоровью микробов) и сохраняют для последующего изучения. Это мудро, потому что аналитические методики – в том числе методики секвенирования («прочтения») геномов – сейчас стремительно развиваются и столь же стремительно дешевеют.
Регулярно проводится и оценка приспособленности. Для этого сравнивают скорость размножения подопытных и контрольных бактерий, причем в роли вторых выступают размороженные предки первых – исходный штамм, из которого были взяты родоначальники всех 12 экспериментальных популяций.
Кишечные палочки выгодно отличаются от баобабов тем, что позволяют Ленски и его коллегам ежегодно получать интересные результаты и публиковать статьи в ведущих журналах. Так, в 2009 году они опубликовали в Nature отчет об эволюции одной из 12 популяций (Barrick et al., 2009). К этому времени длительность эксперимента уже была достаточной для того, чтобы каждая из возможных точечных мутаций (нуклеотидных замен) успела произойти в популяции более одного раза[50].
Авторы следили за темпом закрепления мутаций и изменением приспособленности. Напомним, что возникновение мутации и ее закрепление – не одно и то же. Далеко не всякая возникшая мутация закрепляется (фиксируется) в популяции. Каждая мутация изначально возникает только у одного микроба. Чтобы мутация зафиксировалась, т. е. достигла 100-процентной частоты, потомки этого микроба должны вытеснить всех остальных микробов в своей колбе. Вредная мутация, скорее всего, будет отсеяна отбором. Полезная мутация под действием отбора может закрепиться, но может и случайно потеряться, пока ее носители еще не успели как следует размножиться. Наконец, нейтральные мутации должны фиксироваться с постоянной скоростью, равной скорости мутирования (обо всем этом мы говорили в главе 1).
За первые 20 тыс. поколений в подопытной популяции зафиксировалось 45 мутаций, в том числе 29 однонуклеотидных замен и 16 иных мутаций (вставок, выпадений, инверсий, встраиваний мобильных элементов). Самое интересное, что скорость накопления мутаций на этом этапе была постоянной. Приспособленность вела себя иначе: сначала она быстро росла, а затем ее рост замедлился (см. рисунок).
Постоянная скорость фиксации, согласно теории, характерна для нейтральных мутаций. Однако все 45 мутаций не могли быть нейтральными. Ясно, что по крайней мере некоторые из них были полезными – об этом свидетельствует рост приспособленности. Полученные результаты трудно увязать и с гипотезой о том, что все 45 мутаций были полезными. Ведь в этом случае обе величины – приспособленность и число накопленных мутаций, – скорее всего, должны были бы меняться сходным образом, т. е. или расти с постоянной скоростью, или параллельно замедляться.
Простейшее объяснение состоит в том, что среди 45 зафиксировавшихся мутаций большинство были нейтральными, а некоторые – полезными. Основная масса полезных мутаций зафиксировалась вскоре после начала эксперимента, т. е. после попадания микробов в новые для них условия, к которым они были плохо приспособлены. Но возможности для «полезного мутирования» быстро исчерпались, и в дальнейшем фиксировались в основном нейтральные мутации.
Есть, однако, четыре аргумента против такого объяснения.
1. В случае преобладания нейтральных мутаций должно быть повышено число синонимичных нуклеотидных замен. Вопреки этим ожиданиям все без исключения зафиксировавшиеся мутации в кодирующих областях генов оказались значимыми (несинонимичными). Резкое преобладание значимых замен над синонимичными – это характернейшая «подпись», оставляемая в геноме положительным отбором.
2. В случае преобладания нейтральных мутаций следует ожидать, что во всех 12 экспериментальных популяциях за 20 тыс. поколений мутации зафиксировались в разных генах. Напротив, мутации в одних и тех же генах, закрепившиеся независимо в разных популяциях, будут доводом в пользу того, что мутации фиксировались под действием положительного отбора, а не генетического дрейфа (т. е. мутации были полезными). Чтобы проверить это, авторы отсеквенировали у бактерий поколения № 20 000 из остальных одиннадцати экспериментальных популяций 14 генов, в которых у первой популяции закрепились мутации. Оказалось, что в большинстве случаев в других популяциях эти гены тоже изменились.
3. Если бы большинство мутаций были нейтральными, наблюдалась бы значительная внутрипопуляционная изменчивость по этим локусам (потому что полезные мутации под действием отбора фиксируются быстро, а нейтральные сначала должны долго «случайно блуждать» между нулевой и 100-процентной частотой). Это предположение не подтвердилось.
4. При помощи генной инженерии авторы смогли напрямую определить степень полезности девяти мутаций из рассматриваемых 45. Эти мутации искусственно внедряли в геном предкового штамма. В восьми случаях из девяти приспособленность бактерий резко повысилась[51]. Что касается девятой мутации, то авторы думают, что она тоже полезна, но не сама по себе, а в сочетании с другими мутациями, потому что точно такая же мутация закрепилась у других подопытных популяций.
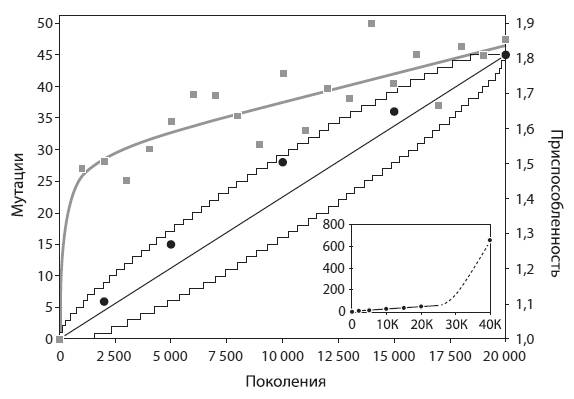
Накопление мутаций (черные линии и кружки) и рост приспособленности (серые линии и квадраты) в экспериментальной популяции. По горизонтальной оси – номер поколения. Видно, что число зафиксировавшихся мутаций росло линейно (тонкие ломаные линии очерчивают 95-процентные доверительные интервалы линейной модели). Приспособленность сначала росла очень быстро, а потом ее рост замедлился. «Прыжки» серых квадратов вверх и вниз относительно серой линии не выходят за пределы статистической погрешности, т. е. не требуют специальных объяснений. На маленьком графике в правом нижнем углу показано резкое ускорение накопления мутаций начиная примерно с поколения № 26 000, когда в популяции зафиксировалась мутация, повышающая темп мутагенеза. Из Barrick et al., 2009.
Таким образом, в течение первых 20 тыс. поколений в популяции фиксировались преимущественно полезные мутации, причем их фиксация шла с постоянной скоростью. Замедление роста приспособленности, очевидно, было связано с тем, что средняя степень полезности мутаций постепенно снижалась. Наиболее радикальные адаптивные изменения произошли в течение первых 2 тыс. поколений, а затем происходила более тонкая настройка.
До сих пор речь шла только о первой половине эксперимента. Во второй его половине эволюционная динамика популяции резко изменилась. Дело в том, что после 26 тыс. поколений зафиксировалась мутация в гене mutT. Этот ген кодирует белок, участвующий в репарации (починке) ДНК. В результате частота мутирования выросла примерно в 70 раз (от 1,6×10−10 до 1,1×10−8 на нуклеотид за поколение). Как следствие, более чем на порядок выросла и частота фиксации мутаций. В течение второй половины эксперимента зафиксировалось 609 мутаций – в 13,5 раза больше, чем за первые 20 тыс. поколений.
Аналогичные мутации, увеличившие темп мутагенеза, закрепились и в нескольких других экспериментальных популяциях. Из этого следует, что рост темпов мутагенеза дал бактериям адаптивное преимущество. Это, между прочим, противоречит распространенной идее о том, что в стабильных условиях организмам было бы выгодно[52] снизить темп мутирования до нуля – и этого не происходит только из-за технической невозможности обеспечить абсолютную точность копирования ДНК.
Мутаторы
Мутации, повышающие скорость мутирования, закрепляются во многих эволюционных экспериментах на бактериях. Гены (точнее, генетические варианты – аллели), несущие такие мутации, называют аллелями-мутаторами или просто мутаторами. Аллелем-мутатором может стать любой ген, нормальная работа которого важна для точной репликации или репарации, если его слегка «подпортит» случайная мутация.
Нужно иметь в виду, что «полезность» мутаторов не прямая, а косвенная. Сама по себе повышенная скорость мутагенеза снижает приспособленность организмов, потому что большинство мутаций, как известно, вредны. Все очень просто: чем интенсивнее мутагенез, тем больше мутаций у потомков и, следовательно, тем ниже их средняя приспособленность. Это и значит, что мутатор не приносит прямой пользы – наоборот, он приносит прямой вред. Косвенная же польза заключается в том, что нет-нет да и возникнет у какого-нибудь носителя аллеля-мутатора редкая, маловероятная полезная мутация. Причем настолько полезная, что ее польза перевесит вред, приносимый мутатором напрямую. Поскольку полезная мутация маловероятна, она скорее возникнет у носителя аллеля-мутатора, чем у организма с низкой скоростью мутирования. В результате адаптивное преимущество получит организм, несущий редкую полезную мутацию, а заодно и аллель-мутатор – в качестве неприятной, но неизбежной «нагрузки». Этот организм и его потомки будут размножаться быстрее других, постепенно вытесняя из популяции конкурентов и распространяя в генофонде обе свои генетические особенности – полезную мутацию и аллель-мутатор. Генетики называют такой способ распространения аллелей hitchhiking – езда автостопом. Имеется в виду, что мутатор «едет автостопом» на полезной мутации, распространяясь в генофонде вопреки тому, что сам по себе он вообще-то вреден.
«Автостоп» прекрасно работает в бесполых популяциях, где связку «полезная мутация – аллель-мутатор» невозможно разорвать. Обычно именно с такими бактериями – бесполыми, нарочно лишенными способности к горизонтальному переносу генов – и работают экспериментаторы. В эксперименте Ленски тоже используются бесполые кишечные палочки. Если бы бактерии могли меняться генами, эволюционные судьбы двух аллелей не были бы столь неразрывными. Обязательно появились бы бактерии, несущие полезную мутацию, но не имеющие мутатора. Эти бактерии стали бы вытеснять тех, у кого два аллеля остались «в связке».
При действующем горизонтальном переносе генов мутатору куда труднее зафиксироваться. Он может даже быть полностью вытеснен из генофонда – конечно, если не успеет до этого момента сгенерировать у кого-то из своих носителей еще одну полезную мутацию.
Мутация, повысившая темп мутагенеза, увеличила вероятность возникновения новых полезных мутаций, когда простые (высоковероятные) пути для этого уже были пройдены. И в этом состояло единственное благо от ускорения мутагенеза. Но при этом в качестве побочного эффекта должно было вырасти число вредных и нейтральных мутаций.
Поэтому следовало ожидать, что теперь большинство фиксирующихся мутаций будут не полезными, а нейтральными. Как мы помним, скорость фиксации нейтральных мутаций в популяции равна скорости мутагенеза. Действительно, в первые 20 тыс. поколений фиксировалось очень мало нейтральных мутаций, а большая часть из 609 «поздних» мутаций оказались нейтральными.
Результаты эксперимента оказались во многом неожиданными. Например, мало кто ожидал, что постоянный темп накопления полезных мутаций может сопровождаться замедляющимся ростом приспособленности или что соотношение темпов фиксации нейтральных и полезных мутаций может так резко меняться. Очевидно, количественные соотношения между разными аспектами эволюционного процесса (нейтральностью и адаптивностью, дрейфом и отбором, темпами изменений на уровне генотипа и фенотипа) могут быть более сложными, неоднозначными и переменчивыми, чем предполагалось.
Как работает эпистаз
Еще об одном интересном результате Ленски и его коллеги сообщили в 2011 году (Waads et al., 2011). Ученые проследили, как организмам удается иногда выходить из «ловушек локального оптимума». Трудно придумать гипотетическую схему, в которой популяция начнет спускаться вниз по ландшафту приспособленности, потому что впереди замаячит более перспективная вершина: ведь спустившиеся особи должны вытесняться менее прозорливыми и ушлыми конкурентами. Но жизнь настойчиво твердит, что ловушки локального оптимума преодолимы, а эксперименты показывают, как это происходит. В итоге победа в эволюционном соревновании достается не тем, кто лучше приспособился здесь и сейчас, а тем, кто, поначалу проигрывая, сохранил лучшие возможности для дальнейшей эволюции. И здесь помогает эпистаз.
Как мы помним, одно из достоинств эксперимента Ленски в том, что часть бактерий периодически замораживают и сохраняют в таком виде для дальнейших исследований. В любой момент их можно оживить и использовать в опытах. Это открывает потрясающие возможности. Например, можно напрямую сравнивать приспособленность ныне живущих бактерий, которые уже более 50 тыс. поколений эволюционировали в своих колбах под присмотром ученых, с их далекими предками. Кроме того, любое эволюционное событие, зарегистрированное в ходе эксперимента, можно многократно «проигрывать заново», размораживая предков и наблюдая, произойдет ли у них это событие снова. Это позволяет отделять случайные и маловероятные события от закономерных и высоковероятных.
Ленски и его коллеги «проиграли заново» эволюцию нескольких подопытных бактерий, замороженных по прошествии 500 поколений основного эксперимента. Все бактерии происходили из одной экспериментальной популяции. К 500-му поколению в этой популяции уже появилось несколько полезных мутаций, которые впоследствии достигли 100-процентной частоты. Кроме того, на этом этапе эксперимента, как и на любом другом, в популяции присутствовали обладатели менее удачных мутаций, которые впоследствии были вытеснены.
Напомним также, что бактерии были лишены генов, разрешающих горизонтальный перенос, так что обмениваться генами, комбинируя удачные варианты, они не могли. Это позволило генетикам выделить среди замороженных микробов поколения № 500 «будущих победителей» – бактерий, обладающих мутациями, которые впоследствии достигли 100-процентной частоты в популяции (будем называть их прапобедителями), и «будущих проигравших» – тех, чьи потомки впоследствии исчезли из популяции (или пралузеров). Выращивали по два штамма каждого типа, т. е. всего четыре линии, выведенные из двух прапобедителей и двух пралузеров.
Размороженные прапобедители имели полезные мутации в генах topA и rbs. Первый ген кодирует фермент топоизомеразу, который помогает расплетать и снова сплетать двойную спираль ДНК в ходе транскрипции (считывания генетической информации). От свойств топоизомеразы зависит активность многих генов. Второй ген, rbs, – это даже не ген, а целый оперон[53], отвечающий за усвоение рибозы.
Мутация topA, характерная для прапобедителей, сама по себе дает 13-процентный выигрыш в приспособленности по сравнению с исходным штаммом бактерий. Это было установлено при помощи генно-инженерных манипуляций: предку «пересадили» эту мутацию, не меняя остального генома, и устроили соревнование. Модифицированный штамм переиграл исходный.
Все мутации в опероне rbs представляют собой делеции (выпадения участков ДНК), дающие выигрыш в 1–2 %. В ходе эксперимента бактерий кормили чистой глюкозой, а не рибозой, поэтому потеря части рибозного оперона могла быть выгодна: она снижала расходы клетки на синтез лишних белков.
У обоих штаммов «проигравших» тоже была мутация в гене topA, но она отличалась от той, что была у прапобедителей. Авторы обозначили ее topA1. Она тоже полезна сама по себе, но повышает приспособленность не на 13, а только на 5 %. У одного из двух штаммов пралузеров была мутация в опероне rbs, и снова не такая, как у прапобедителей. Другие мутации ученым не открылись.
Для начала авторы сравнили приспособленность (скорость роста) штаммов прапобедителей и пралузеров. Казалось бы, у первых приспособленность должна быть выше. Как ни странно, результат оказался противоположным. Выяснилось, что пралузеры превосходят по приспособленности предковый штамм на 20–23 %, тогда как прапобедители опережают предка лишь на 13–15 %. Таким образом, на промежуточном зачете после 500 поколений пралузеры вырвались вперед, сильно обогнав «будущих победителей». Это, конечно же, означает, что у «будущих проигравших» имелись какие-то полезные мутации, которые ученым пока не удалось обнаружить, причем польза от них перекрывает известный выигрыш от мутаций topA и rbs.
Авторы рассчитали, что если бы репродуктивное преимущество пралузеров над прапобедителями, наблюдавшееся после 500-го поколения, сохранялось и впредь, то пралузеры полностью вытеснили бы прапобедителей примерно за 350 поколений, т. е. к 850-му поколению. Как мы знаем, этого не случилось. Все произошло наоборот. Очевидно, потомкам прапобедителей удалось менее чем за 350 поколений приобрести новые полезные мутации, которые позволили им обогнать потомков пралузеров в эволюционном соревновании. Естественно, возникает вопрос: почему потомки пралузеров сами не приобрели аналогичных мутаций, ведь у них было на это ровно столько же времени и хорошая фора?
Авторы предположили, что разгадка может скрываться в различном влиянии мутаций, имеющихся у прапобедителей и пралузеров, на дальнейшие эволюционные перспективы. Эффекты действия генов, в том числе и мутантных, накладываются друг на друга; напомним, что это явление называют эпистазом. Степень полезности той или иной мутации не абсолютна: она зависит от генетического контекста. Скажем, мутация А может быть полезной при наличии мутации Б, но вредной при ее отсутствии (или наоборот). Можно предположить, что полезные мутации, изначально обеспечившие быстрый рост приспособленности у пралузеров, снизили способность бактерий к дальнейшей адаптации. Например, они могли сглаживать или даже сводить на нет эффекты каких-то других, еще не возникших мутаций, полезных в других генетических контекстах. При этом мутации прапобедителей сами по себе были менее полезны, но зато они не закрыли дорогу для будущих приобретений.
Можно ли проверить эту гипотезу? Да! Генетики провели несколько остроумных экспериментов, в которых весьма наглядно показали счастливую мутационную судьбу прапобедителей и злополучную – пралузеров. Мутационное счастье заключалось в повышенной выгоде от новоприобретений, а злосчастье – в пониженной.
Для начала геномы бактерий каждого из четырех штаммов пометили точечными мутациями, не влияющими на приспособленность, но позволяющими различать штаммы по окраске[54]. Затем меченых (белых и красных) бактерий из одного и того же исходного штамма (либо прапобедителей, либо пралузеров) смешивали в соотношении 50:50 и позволяли эволюционировать в тех же условиях, что и в основном эксперименте. В каждом поколении регистрировалось соотношение белых и красных бактерий. До тех пор пока в эволюционирующей популяции не возникало новых полезных мутаций, это соотношение испытывало лишь небольшие случайные колебания под действием генетического дрейфа. Но, как только возникала первая полезная мутация, ситуация резко менялась. Фокус тут в том, что любая полезная мутация изначально возникает у какой-то одной бактерии. «Повезет» либо красной, либо белой бактерии. Потомки бактерии с полезной мутацией начинают быстро размножаться, и, соответственно, в популяции начинает расти доля либо белых, либо красных микробов (точнее, микробов, образующих белые или красные колонии на соответствующей среде). При этом ученые получают сразу две уникальные возможности: 1) с большой точностью поймать момент возникновения первой полезной мутации; 2) оценить степень ее полезности по скорости, с которой соотношение красных и белых будет отклоняться от исходного 50:50.
Нужно подчеркнуть, что речь здесь идет только о первой полезной мутации. Пока полезная мутация всего одна, соотношение белых и красных уходит от исходного состояния по экспоненте и всю ситуацию можно анализировать при помощи достаточно простой математики. Как только появляется вторая полезная мутация, картина становится слишком сложной.
При помощи этой великолепной методики авторы показали, что скорость появления полезных мутаций в линиях прапобедителей и пралузеров одинакова, однако средняя полезность первой полезной мутации, возникающей в штаммах прапобедителей, заметно выше, чем у пралузеров. Иными словами, экспоненциальный рост или снижение соотношения белых и красных у прапобедителей в среднем шли быстрее, чем у пралузеров, вплоть до появления второй полезной мутации, которая «смазывала» картину. У победителей первая полезная мутация повышала приспособленность в среднем на 6 %, а у лузеров – только на 4 %. В прямых конкурентных экспериментах между прапобедителями и пралузерами выяснилось, что первые теперь в среднем на 2,1 % более приспособлены, чем вторые. Это значит, что их победа была не случайностью, а закономерным следствием более высокого «эволюционного потенциала». Это подтверждает предположение о том, что «генетический контекст» у прапобедителей более благоприятен для последующей адаптивной эволюции. Разумеется, полезные возникавшие мутации были разными и далеко не во всех случаях авторам удалось их идентифицировать.
Исследователям удалось расшифровать один конкретный пример взаимного влияния мутаций (эпистаза) из числа тех, что обеспечили итоговый выигрыш прапобедителей. Оказалось, что у них в шести из 20 линий потомков за 883 поколения закрепились полезные мутации в гене spoT – многофункциональном регуляторе активности генов. Мутация в этом гене закрепилась также и в основном долгосрочном эксперименте. Однако ни в одной из 20 линий потомков пралузеров мутации в гене spoT не зафиксировались. При помощи генно-инженерных экспериментов удалось показать, что мутация spoT оказывается полезной в сочетании с мутацией topA, характерной для штаммов прапобедителей, но не приносит пользы в сочетании с мутацией topA1, характерной для пралузеров.
Получается, что тот эволюционный путь, по которому пошли пралузеры, хотя и обеспечил им преимущество на ранних этапах эксперимента, оказался менее перспективным, в частности потому, что лишил бактерий возможности повысить свою приспособленность за счет приобретения мутаций в гене spoT.
Таким образом, в долгосрочной перспективе вероятность закрепления той или иной мутации зависит не только от ее непосредственного влияния на приспособленность «здесь и сейчас», но и от ее воздействия на эволюционные перспективы, т. е. на вероятность того, что другие мутации, которые могут возникнуть в будущем, окажутся полезными. В результате линии, поначалу вырвавшиеся вперед в эволюционной гонке, в конечном счете могут оказаться в проигрыше. Разумеется, для этого необходимо, чтобы отстающие, но перспективные линии успели приобрести дополнительные полезные мутации раньше, чем их полностью вытеснят более успешные конкуренты.
Эти удивительные результаты перекликаются с палеонтологическими фактами, которые подметил еще в XIX веке русский зоолог В. О. Ковалевский (1842–1883), изучавший эволюцию копытных. Палеонтологическая летопись демонстрирует немало примеров того, как из двух конкурирующих групп, возникших примерно в одно и то же время, сначала добивается успеха одна, но затем ее вытесняет другая. При этом адаптивная эволюция в обеих группах идет в одном направлении (у копытных речь шла о преобразованиях стопы и кисти). В первой успешной группе ключевые приспособления развиваются быстрее, но являются более поверхностными, несбалансированными. Во второй группе, которая поначалу занимает подчиненное положение, аналогичные адаптации развиваются медленнее, но в итоге оказываются более комплексными, слаженными и глубокими (Расницын, 1986). Эту закономерность традиционно объясняли на основе общих представлений о «компромиссном» характере эволюции. Любая адаптация покупается ценой ограничения возможностей для развития других адаптаций. Быстро приобретенные «косметические» адаптации могут перекрыть пути дальнейшего совершенствования, так что весь путь в итоге оказывается тупиковым. Теперь мы видим, как эта закономерность работает на молекулярно-генетическом уровне.
Новое устройство враз не прилаживается
По прошествии 31 тыс. поколений в одной из 12 подопытных популяций (ее условное обозначение – Ara-3) произошло что-то странное. Напомним, что бактерий ежедневно пересаживают в колбы с новой питательной средой. Сначала бактерии быстро размножаются, но потом глюкоза в колбе заканчивается, и рост бактерий прекращается – до следующей пересадки. Так было во всех подопытных популяциях, включая Ara-3. Но в один прекрасный день ученые заметили, что численность бактерий этой популяции продолжает расти и после того, как вся глюкоза в колбе уже съедена. К концу суточного цикла численность Ara-3 оказывалась намного выше, чем у остальных популяций. Очевидно, микробы научились использовать в пищу какое-то вещество, входящее в состав среды, но несъедобное для обычных кишечных палочек.
Вскоре Ленски и его коллеги выяснили, что бактерии из популяции Ara-3 приобрели способность питаться цитратом (лимонной кислотой). Цитрат добавляется в среду в качестве вспомогательного вещества. Нормальные бактерии E. coli способны усваивать цитрат только в анаэробных (бескислородных) условиях. Неспособность питаться цитратом в присутствии кислорода – один из определительных признаков данного вида бактерий. Таким образом, на глазах изумленных ученых в популяции Ara-3 появилось настоящее эволюционное новшество – новый полезный признак. Этот признак (авторы обозначили его Cit+) изменил взаимоотношения организма со средой и позволил бактериям-мутантам увеличить свою численность.
Ученые отсеквенировали геномы 29 бактерий из популяции Ara-3, замороженных в разное время. По этим данным было построено их эволюционное дерево (оно показано на рисунке). Оказалось, что популяция оставалась генетически разнообразной на протяжении почти всей своей истории. В ней из одного предкового клона получилось несколько генетически различающихся линий (клад), но они не спешили вытеснять друг друга. Скорее всего, это значит, что большинство различий между кладами были нейтральными, т. е. не влияли на приспособленность.
Удалось выявить конкретное генетическое изменение, которое дало бактериям возможность питаться цитратом. Микробы Cit− превратились в Cit+ благодаря дупликации (удвоению) фрагмента хромосомы, содержащего ген citT. Этот ген кодирует белок, транспортирующий цитрат из внешней среды в цитоплазму бактериальной клетки. В норме у E. coli ген citT активен только в анаэробных условиях. Однако в результате дупликации одна из двух копий citT попала под управление промотора (регуляторного участка) другого, соседнего гена (rnk). При помощи генно-инженерных экспериментов авторы показали, что промотор гена rnk обеспечивает работу контролируемого им гена в аэробных условиях.
Разобравшись с природой ключевой мутации, ученые задались следующим вопросом: было ли появление фенотипа Cit+ в кладе 3 полностью случайным? Могло ли это событие с тем же успехом произойти в другой кладе или в другой популяции, или оно было подготовлено предшествующей эволюцией именно этой клады? В поисках ответа Ленски и его коллеги провели повторные эксперименты с размороженными представителями клад 1, 2 и 3, а также с исходным (предковым) штаммом.
Выяснилось, что у предкового штамма вероятность появления фенотипа Cit+ пренебрежимо мала. Представители клады 1 выработали этот фенотип в двух повторных экспериментах из 55. Это уже лучше! Микробы из клады 2 научились питаться цитратом в двух случаях из 97. Наконец, бактерии из клады 3 приобрели эту способность в восьми случаях из 37 повторных опытов. Еще лучше! Похоже на то, что вероятность приобретения нового полезного свойства росла постепенно. Дополнительные эксперименты подтвердили этот вывод.
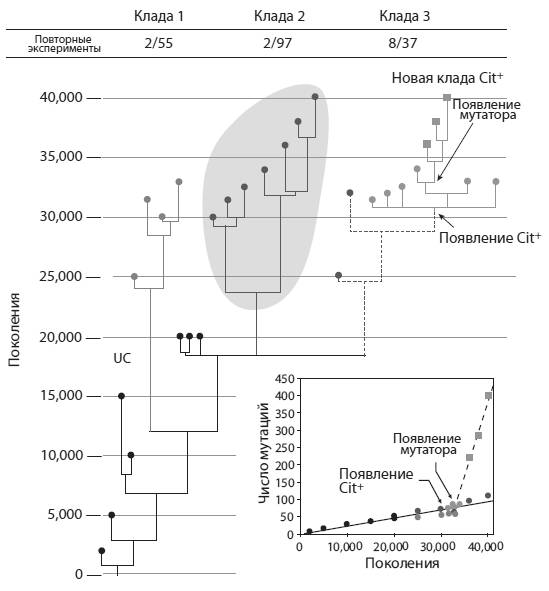
Эволюционная история популяции Ara-3, в которой бактерии научились питаться цитратом. Числа слева – поколения. Кружками на дереве обозначены 29 клонов, чьи геномы были отсеквенированы. На дереве выделяются пять основных клад (эволюционных линий): UC (unsuccessful clade, быстро вымершая ранняя линия), клада 1, клада 2, клада 3 («потенцированные» клады с повышенной вероятностью появления фенотипа Cit+, т. е. способности питаться цитратом), новая клада Cit+ – клада, способная питаться цитратом, произошедшая от клады 3 после 31 тыс. поколений (Появление Cit+). После 33 тыс. поколений у бактерий Cit+ появилась мутация, резко повышающая темп мутагенеза (Появление мутатора). В верхней части рисунка показаны результаты повторных эволюционных экспериментов с замороженными представителями клад 1, 2 и 3. Представители клады 1 выработали фенотип Cit+ в двух случаях из 55 попыток, клады 2 – в двух случаях из 97, клады 3 – в восьми случаях из 37. Представители исходного предкового штамма имеют пренебрежимо малую вероятность появления фенотипа Cit+. График справа внизу показывает темп накопления мутаций, резко увеличившийся у бактерий Cit+ (светло-серые кружки) после появления аллеля-мутатора. Из Blount et al., 2012.
Приобретение фенотипа Cit+ во всех случаях было связано с тем, что ген citT начинал экспрессироваться в аэробных условиях. Но достигался этот результат разными путями. В некоторых повторных опытах, как и в основном долгосрочном эксперименте, произошли тандемные дупликации[55], благодаря которым citT оказался под управлением аэробного промотора. Но границы дуплицированных участков в разных случаях были разными, а промотор, взявший на себя управление геном citT, не всегда был промотором гена rnk: в одном случае это был промотор другого гена (rna). В нескольких повторных опытах тот же эффект был достигнут без дупликации – благодаря встраиванию мобильного генетического элемента IS3 в кодирующую часть гена, расположенного по соседству с citT. В этом мобильном элементе как раз имеется подходящий промотор, взявший на себя управление геном citT.
Повторные эксперименты подтвердили, что вероятность приобретения признака Cit+ росла в ряду «предковый штамм – клады 1 и 2 – клада 3». Стало быть, появление этого признака именно в кладе 3 не было простой случайностью. Микробы были заранее подготовлены к этому – «потенцированы». Иными словами, у них в ходе предшествующей эволюции зафиксировались какие-то мутации, которые сами по себе не давали возможности питаться цитратом, но повысили вероятность развития этой способности в будущем. Разумеется, «потенцирующие» мутации зафиксировались не потому, что микробы планируют свою эволюцию наперед. Эти мутации либо были нейтральными и зафиксировались случайно, либо были полезны для чего-то другого. Подготовка к цитратному питанию была побочным эффектом, которого естественный отбор не мог предусмотреть.
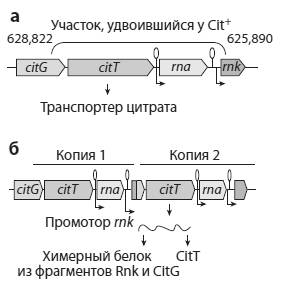
Дупликация, которая привела к появлению способности питаться цитратом у бактерий из популяции Ara-3. а – участок хромосомы предкового штамма, б – тот же участок после дупликации. Стрелками и петельками обозначены промоторы генов rna и rnk, обеспечивающие работу этих генов в аэробных условиях. В результате дупликации ген citT, кодирующий транспортер цитрата, оказался под управлением промотора гена rnk и стал экспрессироваться в присутствии кислорода. Из Blount et al., 2012.
Следующими экспериментами удалось доказать, что какие-то генетические особенности клады 3 действительно способствуют эффективному питанию цитратом. Чтобы убедиться в этом, исследователи вставили в геномы представителей предкового штамма и клад 1–3 по несколько копий гена citT под управлением аэробного промотора. Иными словами, они придавали микробам способность поглощать цитрат – и смотрели, насколько микробы расположены к новой диете.
Представители всех генно-модифицированных штаммов в результате научились использовать цитрат в пищу, но в очень разной степени. Микробы из клады 3 делали это лучше всех: они быстро переключались с глюкозы на цитрат и хорошо росли на чистом цитрате. Микробы из клад 2 и 1 справлялись хуже: им требовалось больше времени на переключение, и росли на цитрате они медленнее. Предковый штамм использовал цитрат еще менее эффективно. Для того чтобы после исчерпания запасов глюкозы переключиться на питание цитратом, ему требовалось около двух суток. Между прочим, это означает, что в условиях долгосрочного эксперимента он не получил бы никакого преимущества от мутации, которая создала фенотип Cit+ в кладе 3: никто не дал бы ему двух суток на раздумья, ведь бактерий пересаживают в новую среду с глюкозой каждые сутки.
Эти результаты, как и повторные эволюционные эксперименты, показывают, что «потенцирование» проходило как минимум в два этапа. Вероятность формирования фенотипа Cit+ выросла при переходе от предкового штамма к кладам 1 и 2 и снова увеличилась при формировании клады 3.
Интересно, что первые бактерии, у которых после поколения № 31 000 был зарегистрирован фенотип Cit+, использовали цитрат еще очень неэффективно, хотя у них уже были и «потенцирующие» мутации, и тандемная дупликация. Новая функция поначалу была несовершенна и давала лишь едва заметное преимущество. В ходе дальнейшей эволюции эффективность использования цитрата микробами Cit+ быстро росла. Исследователям удалось расшифровать один из механизмов усовершенствования: фрагмент ДНК с активированным геном citT просто-напросто подвергся еще нескольким дупликациям. Это, по-видимому, ускорило поглощение цитрата из внешней среды.
Таким образом, формирование эволюционного новшества происходило в три этапа. На первом этапе (потенцирование) закрепились мутации, повысившие вероятность появления признака в будущем. На втором этапе (актуализация) появилась и была поддержана отбором ключевая мутация, превратившая микробов Cit− в Cit+. Правда, поначалу новый признак был слабо выражен и почти не приносил пользы. На заключительном, третьем этапе (усовершенствование) признак постепенно оптимизировался. В результате его полезность многократно выросла.
Усовершенствование – процесс, который может продолжаться долго. Однако события, происходившие в популяции Ara-3 после поколения № 35 000, трудно анализировать. В это время среди микробов Cit+ (как и во многих других подопытных линиях) распространилась мутация, повышающая скорость мутагенеза в 20 раз, – уже знакомый нам аллель-мутатор. Найти среди сотен новых мутаций те, что связаны с усовершенствованием цитратного питания, – задача пока слишком трудная. Впрочем, замороженные бактерии никуда не спешат и будут спокойно ждать появления новых методов и приборов (Blount et al., 2012).
- Интересующийся
Исключительная слабость, заключающаяся в фактически полном отсутствии каких-либо научных свидетельств естественного происхождения жизни где-то во Вселенной — это тщательно сохраняемый секрет нашей официальной науки, образования и средств массовой информации.
У верующих может не хватить знаний, чтобы разоблачить хитроумные наукообразные фокусы эволюционистов или написанные тяжелым научным слэнгом нечестные объяснения. Но когда эволюционисты имеют дело с подготовленными учеными-креационистами, они разводят руками и вынуждены признаться, что научных доказательств эволюционной теории нет.
Я читал немало диалогов учёных с креационистами, и как правило всё сводится к невежеству последних. Креационисты "опровергли" ТЭ только в среде своих сторонников. Никто, ни одного учёного не заставляет "верить" в ТЭ, это вопрос не веры, а знания! Знание на стороне ТЭ, поэтому её "альтернативу" - креационизм, как правильно заметил Галиций, не преподают в ВУЗ-х и школах. Удел креационизма обитать на задворках науки и в умах не подготовленных обывателей.
Это говорит о том, что данная научная проблема сложная, но имеющая решение... Вам уже Галиций намикал, что проблемы абиогенеза и ТЭ - это немного разные темыВ конце вашей ссылки, Димитрий, есть цитата: "Как пишет Пригожин, "старая проблема происхождения жизни предстает в новом свете. Заведомо ясно, что жизнь несовместима с принципом порядка Больцмана, но не противоречит тому типу поведения, который устанавливается в сильно неравновесных условиях", и далее: "Разумеется, проблема происхождения жизни по-прежнему остается весьма трудной, и мы не ожидаем в ближайшем будущем сколько-нибудь простого ее решения. Тем не менее, при нашем подходе жизнь перестает противостоять "обычным" законам физики, бороться против них, чтобы избежать предуготованной ей судьбы - гибели."
Это говорит о том, что у науки нет доказательств эволюционного происхождения жизни. Что и требовалось доказать.
- Православный христианин
Потому и не спорят, что не православные христиане! И нам они не указ.Теория эволюции не отрицает Бога. Католики же не спорят.
А насчет ТЭ, так это ложь!
Нет уж, дорогой вы наш!Библия как Святое Писание собрано Православной Церковью и эта книга откровение для верующих, а не научная в вашем понимании. Читать её может каждый, а вот понять и толковать - лишь тот, кому будет дано Святым Духом. Иные же (иудеи и язычники) не понимают эти книги и для них сказанное в них: либо соблазн, либо безумие. Под язычниками понимаем атеистов - дарвинистов.. А Библию каждый толкует как ему нравится. Библия не для буквального понимания. Это не книга научная, научных открытий по которую надо подгонять науку.
Александр Марков - это активный деятель движения "Брайтс", который ничего общего с наукой не имеет, а лишь популяризатор идеи "Брайтов" в России Хватит нам пичкать сюда богоборцев, их мнение уж точно не может быть опровержением Креационизма.Александр Марков "Эволюция"
- Православный христианин
А кто вы такой, чтобы ставить оценки?Я читал немало диалогов учёных с креационистами, и как правило всё сводится к невежеству последних
Дмитрий, вас спросили про вашу ученую степень. Может раскроете?
Патриарх не так давно прощупывал православных на предмет объединения с католиками.Потому и не спорят, что не православные христиане! И нам они не указ.
А насчет ТЭ, так это ложь!
Основное разногласие это папство как гарант истинности христианского учения.
Если этот вопрос будет решён, то объединения с католиками будет очень актуальным.
Остальные противоречия по дарвину и инопланетянам снимутся автоматически как несущественные.
Кто хочет пусть верит.
Те православные которые Духом Святым живут, такой ерундой как вопросами о создании мира и т.п. не занимаются. Они учат как дойти до вершин духа. И совсем другие вопросы ставятся и толкуются, которые большинству скорее всего не интересно.Нет уж, дорогой вы наш!Библия как Святое Писание собрано Православной Церковью и эта книга откровение для верующих, а не научная в вашем понимании. Читать её может каждый, а вот понять и толковать - лишь тот, кому будет дано Святым Духом. Иные же (иудеи и язычники) не понимают эти книги и для них сказанное в них: либо соблазн, либо безумие. Под язычниками понимаем атеистов - дарвинистов.
- Статус
- В этой теме нельзя размещать новые ответы.
Поделиться: